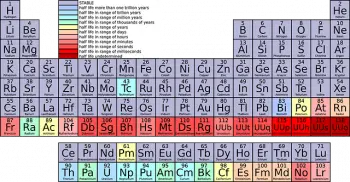
La taula periòdica dels elements químics és una de les eines més poderoses i essencials en la química i la ciència en general. Entre les seves característiques més distintives hi ha les "famílies" o els "grups" en què els elements químics s'organitzen d'acord amb les seves propietats similars.
Abans de submergir-nos a les famílies específiques de la taula periòdica, és important comprendre la seva organització general:
Què són les famílies de la taula periòdica?
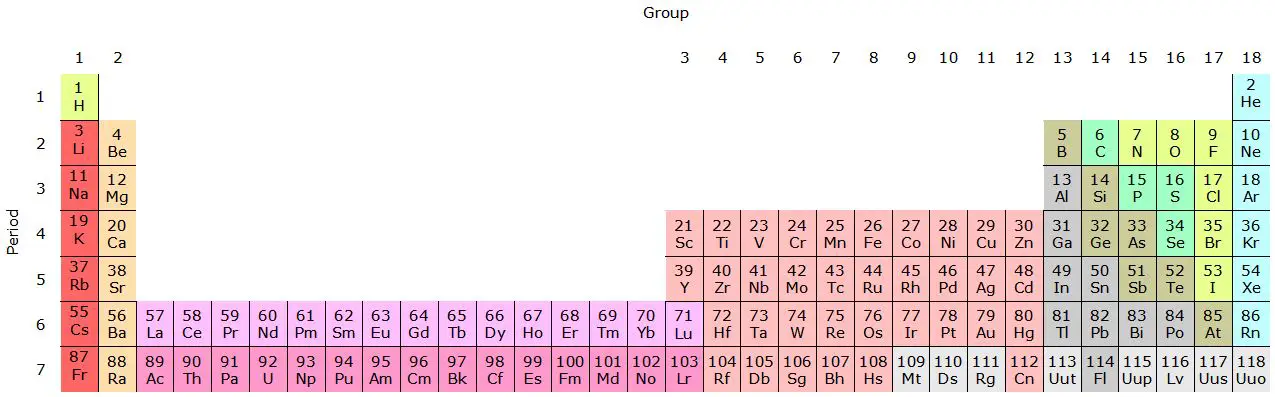 Les famílies de la taula periòdica són grups verticals d'elements amb propietats químiques similars a causa de la configuració electrònica compartida a la capa més externa d'electrons.
Les famílies de la taula periòdica són grups verticals d'elements amb propietats químiques similars a causa de la configuració electrònica compartida a la capa més externa d'electrons.
La taula periòdica es divideix en files horitzontals anomenades "períodes" i columnes verticals anomenades "grups" o "famílies". Els elements s'organitzen en ordre creixent de nombre atòmic, que és la quantitat de protons al nucli d'un àtom.
Els elements de cada família comparteixen característiques i propietats químiques semblants. Cada família té un número específic i s'identifica amb un número romà o un número ordinal (per exemple, el Grup I o el Grup 1).
Per què s'organitzen els elements en famílies?
A la dècada de 1860, Dmitri Mendeléyev estava intentant ordenar els elements coneguts en funció de les seves propietats i masses atòmiques.
Durant aquest procés, va notar que quan els elements s'organitzaven en files en ordre creixent de les masses atòmiques, es produïen patrons repetitius de propietats químiques similars a cada certa quantitat d'elements.
Això ho va portar a la idea que els elements haurien d'organitzar-se en columnes o famílies, on els elements a la mateixa columna tindrien propietats químiques similars.
Les famílies més importants de la taula periòdica
Família 1: Els metalls alcalins
 Els metalls alcalins són els elements del grup 1 de la taula periòdica, que inclou l'hidrogen (H), el liti (Li), el sodi (Na), el potassi (K), el rubidi (Rb), el cesi (Cs ) i el franci (Fr).
Els metalls alcalins són els elements del grup 1 de la taula periòdica, que inclou l'hidrogen (H), el liti (Li), el sodi (Na), el potassi (K), el rubidi (Rb), el cesi (Cs ) i el franci (Fr).
Propietats bàsiques
Aquests elements són altament reactius i tendeixen a perdre un electró per formar ions positius. Són coneguts per la seva capacitat per reaccionar vigorosament amb l'aigua i produir hidrogen gasós.
Ús i aplicacions
Els metalls alcalins troben aplicacions a diverses àrees, des de bateries d'ions de liti en dispositius electrònics fins a la fabricació de vidre i la síntesi de compostos químics.
Família 2: Els metalls alcalinoterris
La família dels metalls alcalinoterris comprèn els elements del grup 2 de la taula periòdica, que inclou el beril·li (Be), el magnesi (Mg), el calci (Ca), l'estronci (Sr), el bari (Ba) i el ràdio (Ra).
Propietats bàsiques
Aquests elements també són metalls, però són menys reactius que els metalls alcalins. Tenen dos electrons a la seva capa més externa i tendeixen a perdre aquests dos electrons en les reaccions químiques.
Ús i aplicacions
Els metalls alcalinoterris són essencials per a l'estructura dels ossos i dents (calci), la fabricació d'aliatges metàl·lics (magnesi) i la tecnologia nuclear (ràdio).
Família 17: Els halògens
 Els halògens formen la família 17 de la taula periòdica i inclouen el fluor (F), el clor (Cl), el brom (Br), el iode (I) i l'àstat (At).
Els halògens formen la família 17 de la taula periòdica i inclouen el fluor (F), el clor (Cl), el brom (Br), el iode (I) i l'àstat (At).
Propietats bàsiques
Aquests elements són altament reactius i tendeixen a guanyar un electró per formar ions negatius. Són coneguts per la seva capacitat per formar compostos iònics amb els metalls alcalins i alcalinoterris.
Ús i aplicacions
Els halògens troben aplicacions en la desinfecció de l'aigua (clor), la fabricació de productes farmacèutics (iode) i en la fotografia (bromur de plata).
Família 18: Els gasos nobles
La família dels gasos nobles, també coneguda com a gasos inerts, inclou l'heli (He), el neó (Ne), l'argó (Ar), el criptó (Kr), el xenó (Xe) i el radó (Rn).
Propietats bàsiques
Aquests elements són coneguts per la seva baixa reactivitat química pel fet que tenen una capa delectrons completament plena.
Ús i aplicacions
Aquesta estabilitat fa que els gasos nobles siguin útils en aplicacions com llums de neó, refrigeració criogènica i llums de senyalització.
Família dels lantànids i actínids
A la part inferior de la taula periòdica, trobem dues sèries d'elements coneguts com a lantànids i actínids. Els lantànids són elements del bloc f, mentre que els actínids són elements del bloc f.
Els lantànids i actínids són dues sèries d'elements ubicades a la part inferior de la taula periòdica, i sovint se'ls exclou de la numeració de grups o famílies típica de la taula principal. Aquestes sèries es coneixen com a "sèries internes" o "sèries f". Aquestes sèries d'elements sovint s'anomenen "terres rares" a causa de la seva relativa raresa a l'escorça terrestre.
Encara que els lantànids i actínids no es numeren tradicionalment com a grups a la taula periòdica, de vegades se'ls assignen números romans o s'esmenten com a "Grup 3" per als lantànids i "Grup 4" per als actínids com una forma simplificada de referir-s'hi .
Ús i aplicacions
Els lantànids són utilitzats en la fabricació d'imants potents, catalitzadors químics i en la indústria de l'electrònica. D'altra banda, els actínids, incloent elements com l'urani i el plutoni, són molt importants en la tecnologia nuclear i la generació d'energia.
Altres Famílies
A més de les famílies esmentades anteriorment, hi ha altres grups d'elements a la taula periòdica amb característiques i propietats úniques.
Per exemple, el grup 3 conté els "lantànids lleugers" i el grup 16 conté els "calcògens", que inclouen oxigen, sofre i seleni.
