El calci, un element químic essencial per a la vida, és conegut pel seu paper en la salut dels ossos i dents. Tot i això, la rellevància del calci va més enllà de la biologia humana i s'estén a una àmplia gamma de camps científics.
La massa atòmica del calci és un concepte físic i químic que fa referència a la massa mitjana de tots els isòtops de calci que es troben a la natura, ponderada per la seva abundància relativa.
La massa atòmica s'expressa en unitats de massa atòmica unificada (uma) o daltons (Da), i per al calci, la massa atòmica mitjana és d'aproximadament 40.078 u.
Càlcul de la massa atòmica del calci
La massa atòmica del calci es calcula tenint en compte l'abundància relativa dels isòtops naturals.
El calci té diversos isòtops, sent el més abundant el calci-40 (Ca-40), que representa aproximadament el 96% de tot el calci natural. A més, el calci-44 (Ca-44) és un altre isòtop comú, constituint aproximadament el 2.1% del calci natural. Altres isòtops de calci, com el Ca-42 i el Ca-48, són menys abundants i tenen un efecte menor a la massa atòmica mitjana.
El càlcul de la massa atòmica es fa multiplicant la massa de cada isòtop per la seva abundància relativa i sumant-ne els resultats. En el cas del calci, això dóna com a resultat una massa atòmica mitjana al voltant de 40.078 u.
Taula amb les masses atòmiques dels isòtops de calci
La taula següent mostra la massa atòmica de cada isòtop de calci i el percentatge de la seva composició isotòpica.
|
Isòtop |
Massa atòmica (Da) |
Abundància isotòpica (fracció de quantitat) |
|
40 Ca |
39.962 5909 (2) |
96.941% (156) |
|
42 Ca |
41.958 618 (1) |
0.647% (23) |
|
43 Ca |
42.958 766 (2) |
0.135% (10) |
|
44 Ca |
43.955 482 (2) |
2.086% (110) |
|
46 Ca |
45.953 69 (2) |
0.004% (3) |
|
48 Ca |
47.952 5229 (6) |
0.187% (21) |
Propietats i característiques del calci
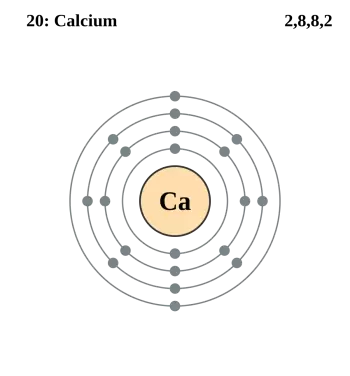
 El calci (Ca) és un element químic de la taula periòdica amb un nombre atòmic de 20. Aquest nombre atòmic indica que un àtom de calci posseeix 20 protons al nucli i, en conseqüència, 20 electrons que orbiten al seu voltant.
El calci (Ca) és un element químic de la taula periòdica amb un nombre atòmic de 20. Aquest nombre atòmic indica que un àtom de calci posseeix 20 protons al nucli i, en conseqüència, 20 electrons que orbiten al seu voltant.
La forma pura del calci és un metall alcalinoterri de color blanc platejat, conegut per la seva reactivitat i el seu caràcter tou. Va ser el 1808 quan Sir Humphry Davy va aconseguir aïllar-lo en la seva forma pura per primera vegada.
A causa de la seva elevada activitat química, el calci no es troba de manera lliure a la natura. Tot i això, és possible obtenir calci metàl·lic pur mitjançant el procés d'electròlisi d'una massa fosa.
El calci ocupa el cinquè lloc a la llista d'elements més abundants a la Terra, després de l'oxigen, el silici, l'alumini i el ferro. A més, és un element que es troba en gran quantitat a l'aigua de mar, amb una concentració aproximada de 400 mg/l. De fet, és al voltant del 3,38% de la massa total de l'escorça terrestre.
Aquest element químic pertany al grup dels metalls alcalinoterris i comparteix la seva alta activitat química amb altres membres daquest grup de la taula periòdica. Tot i la seva activitat, hi ha altres metalls alcalins que són encara més reactius.
A la natura, el calci es troba comunament associat amb diòxid de carboni, oxigen i humitat presents a l'aire, cosa que contribueix a la seva presència en diverses formes i compostos al nostre entorn.
Importància de la massa atòmica del calci
La massa atòmica del calci és un concepte de gran importància a la química, la física i la biologia. Aquesta magnitud no sols és essencial per a la comprensió de les propietats i el comportament del calci en si, sinó que també té nombroses aplicacions en diferents camps científics.
- En química, la massa atòmica del calci es fa servir per calcular la massa molar de compostos que contenen calci. La massa molar és crucial per a la formulació de substàncies i la comprensió de les proporcions a les reaccions químiques. Per exemple, al carbonat de calci (CaCO₃), la massa molar es calcula sumant la massa del calci, el carboni i l'oxigen, cosa que permet determinar la quantitat de substància present en una mostra.
- En física nuclear, la massa atòmica del calci és fonamental per calcular lenergia denllaç dels nuclis atòmics. Lenergia denllaç és necessària per entendre processos com la fissió i la fusió nuclears, que són fonamentals tant en aplicacions energètiques com en la comprensió de lestructura de la matèria.
- En astrofísica, la massa atòmica del calci és rellevant a la nucleosíntesi estel·lar, on es formen elements més pesats a partir d'elements més lleugers a l'interior de les estrelles. El calci es produeix en aquest procés, i la seva massa atòmica contribueix a explicar l'abundància de calci a l'univers i com es formen els elements.
- En biologia, el calci és essencial per a la salut dels éssers vius, incloent-hi els éssers humans. La massa atòmica del calci és clau per calcular la quantitat de calci necessària a la dieta i comprendre el seu paper en la formació d'ossos, la transmissió de senyals nerviosos i moltes altres funcions biològiques.
